Autores: Zapata Cuevas María Alejandra, Cárdenas Belaunzarán Jorge, Galván Chávez Mauricio y Neri Rodríguez Laura Rebeca.
Paciente masculino de 63 años de edad, originario y residente de Ayotlán, Jalisco, México, quien ingresó a la Asociación para Evitar la Ceguera en México I.A.P. “Hospital Dr. Luis Sánchez Bulnes” en mayo de 2018, refiriendo disminución de agudeza visual de rápida evolución en el ojo izquierdo, percibida por primera vez en marzo del mismo año.
Como antecedentes personales patológicos de importancia refiere hipertensión arterial sistémica de un año de diagnóstico en tratamiento con Losartán, Hidroclorotiazida y Ácido acetilsalicílico. También refiere ingesta diaria de Clonazepam por insomnio y hemorroidectomía realizada en 2003.
En cuanto a los antecedentes oftalmológicos, fue operado de FACO + LIO en ojo derecho en noviembre de 2016. En marzo de 2018, inició con disminución de agudeza visual en ojo izquierdo, motivo por el cual fue operado de FACO + LIO en ese ojo, sin presentar mejoría. En ese mismo mes, se le diagnosticó Degeneración Macular Relacionada con la Edad tipo seca, por lo que inició tratamiento con antioxidantes, una tableta cada 24 horas.
Debido a la baja agudeza visual persistente, a pesar de la cirugía de catarata y a la ausencia de mejoría en el ojo izquierdo, el paciente decidió acudir a la Institución para una segunda valoración. En la interrogatorio refirió episodios intermitentes de cefalea hemicraneana opresiva izquierda, intensidad 6/10 que no mejoraba con la ingesta de AINEs de aproximadamente tres meses de evolución, con aumento en la frecuencia y duración de los episodios.
Exploración física
A su llegada al hospital el paciente se encontraba consciente, orientado en sus tres esferas neurológicas y cooperador, con marcada ansiedad. La refracción en ojo derecho de -0.25 de esfera y en ojo izquierdo de +0.25 esferas con -1 de cilindro a 60°. La agudeza visual en ojo derecho de 20/25 y en ojo izquierdo de cuenta dedos a un metro, con presión intraocular de 13mmHg en el ojo derecho y de 15mmHg en el ojo izquierdo. Ambos ojos sin limitación en los movimientos oculares, el segmento anterior se encontraba sin alteraciones, con ángulo abierto en los cuatro cuadrantes y pupilas regulares de forma bilateral, con defecto pupilar aferente en el ojo izquierdo e hiporreactividad de pupila izquierda. El lente intraocular en ambos ojos se encontraba en cámara posterior, en bolsa y sin datos de opacidad capsular posterior. En polo posterior, papila 5/10, con bordes regulares y definidos, mácula con presencia de drusas pequeñas y medianas de tipo duro en ambos ojos, la retina periférica sin presencia de alteraciones.
Como resultado de la refracción obtenida mediante el autorefractor, se descartó desde un inicio que se tratara de un error en el cálculo del lente intraocular del ojo izquierdo, por lo que se solicitó la realización de una tomografía de coherencia óptica (OCT) macular para complementación diagnóstica.
Estudios Complementarios
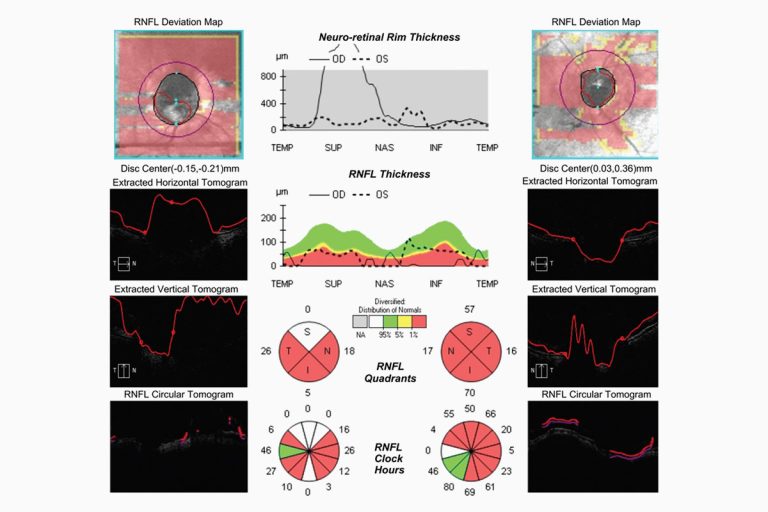
Se realizó un OCT (Cirrus OCT, Carl Zeiss) macular en el que se apreció la presencia de drusas duras y áreas de atenuación focal en el complejo EPR Coriocapilar de ambos ojos. En ojo derecho el resto de las capas de la retina presentaban organización y grosor conservados, mientras que en el ojo izquierdo se observó la presencia de una membrana epirretiniana en región temporal superior periférica que no generaba tracción, con el resto de las capas de la retina sin alteraciones. Ya que su localización era periférica y no condicionaba tracciones, la presencia de dicha membrana epirretiniana no parecía ser justificación suficiente para la mala agudeza visual marcadamente asimétrica entre ambos ojos, motivo por el cual se decidió realizar unos Campos Visuales 30-2.
En los campos visuales (Humphrey Field Analyzer II, Carl Zeiss) blanco-blanco, 30-2, se observó una disminución leve de la sensibilidad en cuadrante temporal superior en el ojo derecho; el ojo izquierdo presentó reducción generalizada de la sensibilidad y desviación total del modelo. Con dicho resultado, se solicitaron campos visuales cinéticos manuales y una resonancia magnética con contraste de gadolinio de cráneo y órbitas.
En los campos visuales cinéticos manuales en ojo derecho se observó con estímulo III4e una reducción concéntrica de predominio superior, inferior y temporal de 10°, sin aumento de mancha ciega. En ojo izquierdo se observó una disminución concéntrica de la sensibilidad con estímulo III4e de aproximadamente 20° y un escotoma central con estímulo III4e en los 10° centrales, sin presentar aumento de mancha ciega.
La resonancia magnética con contraste de gadolinio se realizó a los 10 días de la visita inicial del paciente, y reveló una lesión vascular dilatada adyacente a la superficie dorsal y medial del segmento supraclinoideo para-oftálmico de la carótida interna izquierda, con características de un aneurisma sacular, el cual generaba compresión y deformidad del segmento intracraneal del nervio óptico izquierdo, así como de la parte central e izquierda del quiasma, ambos con señal conservada. El nervio óptico derecho se encontraba sin alteraciones, sin datos de refuerzo anómalo.
Diagnóstico
Con dichos estudios y la presentación clínica del paciente se realizó el diagnóstico de neuropatía óptica compresiva de nervio óptico izquierdo y quiasma óptico secundaria a aneurisma de carótida interna supraclinoidea izquierda.
Tratamiento y seguimiento
Debido al diagnóstico realizado y del riesgo que éste implica para la vida del paciente, se realizó su referencia a un centro médico de neurocirugía para su tratamiento.
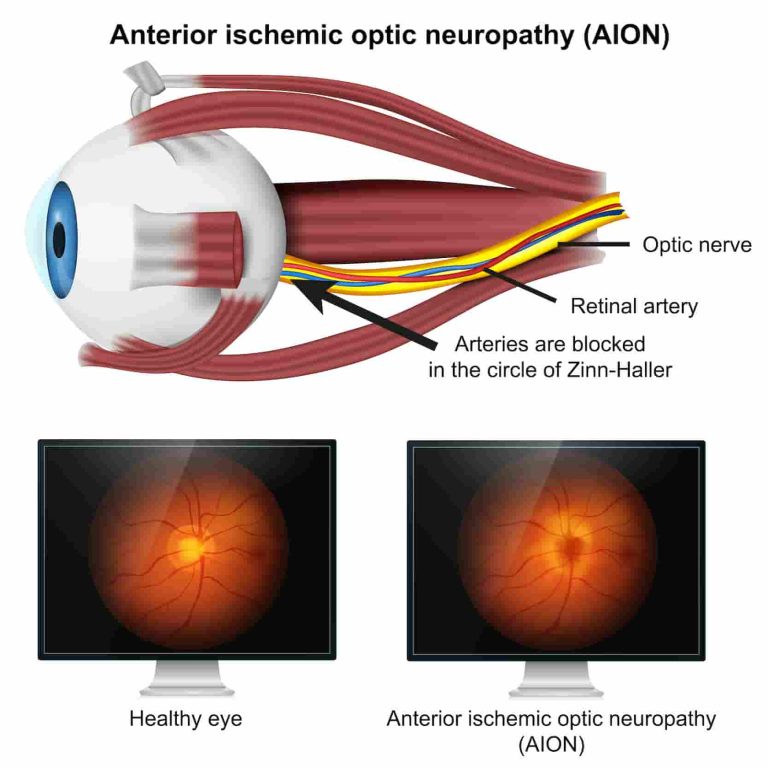
El término neuropatía óptica hace referencia a una lesión del nervio óptico secundario a múltiples etiologías. El daño y la muerte de las células del nervio óptico se ven reflejados en la presentación clínica característica de la neuropatía óptica con baja visual, discromatopsia, defecto campimétrico y defecto pupilar. Si el daño es persistente o irreversible el resultado final es la atrofia óptica.
Las neuropatías ópticas compresivas se encuentran entre las patologías más importantes que afectan la vía visual anterior y que pueden llevar a daño severo en la función visual del paciente si son descubiertas tardíamente.
La pérdida visual que conllevan las neuropatías ópticas compresivas relacionada con patologías de la base del cráneo suele ser incapacitante para los pacientes. Las etiologías más frecuentes incluyen tumores hipofisarios, meningiomas y craneofaringiomas; en menor frecuencia también se presentan aneurismas carotídeos, quistes de bolsa de Rathke, mucoceles sinusales, displasias fibrosas y tumores poco frecuentes de la base del cráneo.
Respecto a los aneurismas intracraneales no rotos, éstos afectan hasta al 5% de la población general. Con frecuencia su diagnóstico se realiza como un hallazgo incidental en una angiorresonancia o una angiotomografía realizada durante la investigación de algún síntoma inespecífico. Cerca del 8% de estos pacientes presentará un síndrome clínico neuro-oftalmológico.
Debido a que el nervio óptico se encuentra localizado cerca de la arteria cerebral anterior, la arteria comunicante anterior, la arteria oftálmica y la porción supraclinoidea de la carótida interna, los aneurismas de estas arterias pueden causar neuropatías ópticas compresivas. De este modo, una lesión aneurismática siempre debe ser considerada como una causa posible de neuropatía óptica compresiva asociada a deterioro visual progresivo.4 Con mayor frecuencia, los aneurismas surgen de la arteria carótida interna, ya sea en el segmento intracavernoso o del segmento supraclinoideo.
Se considera que el mecanismo fisiopatológico del deterioro visual progresivo es la compresión directa sobre el nervio óptico o el quiasma que genera el bloqueo de la conducción nerviosa y desmielinización de las fibras, así como restricción del suministro sanguíneo del nervio por el efecto de masa del aneurisma y en caso de ruptura el sangrado directo en el nervio óptico.
En la mayoría de las ocasiones los aneurismas intracraneales suelen ser asintomáticos hasta el momento de su ruptura, con consecuencias catastróficas para el paciente. La cefalea, el dolor orbitario, la enfermedad cerebrovascular isquémica, las alteraciones en nervios craneales, los síntomas de efecto de masa y la pérdida visual son síntomas que pueden advertir al clínico de un aneurisma intracraneal no roto.6 Entre otros síntomas posibles también se encuentran el dolor orbitario, así como la demencia y alteraciones en la personalidad en algunas ocasiones. 4
El patrón de defectos visuales causados por la neuropatía óptica compresiva aneurismática es variado, pero el compromiso bilateral demostrado mediante los defectos hemianópticos es frecuente.4 Además, la compresión ejercida sobre los diferentes niveles del sistema visual por las masas en la órbita y el cerebro puede condicionar clínicamente un aumento de la excavación papilar y generar una marcada asimetría en el disco con ausencia de correlación entre el disco óptico y los defectos del campo visual.6 En conjunto, las alteraciones perimétricas y la excavación papilar de la neuropatía óptica compresiva pueden ser confundidas con glaucoma.7
Otra de las características más importantes y reveladoras en la presentación clínica de una neuropatía óptica compresiva secundaria a un aneurisma es la rapidez de la instauración de los defectos visuales 7, como en el caso de nuestro paciente, quien reportó la disminución de la agudeza visual de rápida instauración. Asimismo, otro dato clínico importante es la palidez del anillo neurorretiniano, la cual se encuentra presente hasta en el 94% de los casos, y tiene una especificidad para neuropatía óptica no glaucomatosa del 70%.7 A pesar de lo anterior, en el caso de nuestro paciente que contaba con tres meses de evolución, dicha palidez aún no fue observada.
Los aneurismas de la porción intracraneal inicial de la carótida interna pueden imitar otras causas de neuropatía óptica, las cuales deben ser tomadas en consideración.6 Dentro de los diagnósticos diferenciales que también se pueden presentar con una excavación grande, una presión intraocular normal y una rápida disminución de la agudeza visual, se encuentran el glaucoma normotensivo, las neuropatías ópticas desmielinizantes, las neuropatías ópticas arteríticas, las neuropatías ópticas infecciosas, la neuropatía óptica de Leber y la neuropatía óptica traumática. En esos casos, el contexto clínico del paciente y los resultados de los estudios paraclínicos orientarán el diagnóstico.7
Los aneurismas intracraneales que surgen en la región del seno cavernoso o del segmento de la arteria carótida interna, siempre deben ser considerados como etiología ante una pérdida rápidamente progresiva de visión monocular.5 Los estudios de neuroimagen deben ser realizados en los casos de neuropatía óptica compresiva rápidamente progresiva, para descartar una lesión aneurismática, incluso en casos de neuropatía óptica sin ninguna manifestación de dolor. 4
Usualmente el tratamiento preferido para la neuropatía óptica compresiva es la descompresión quirúrgica.2 En el caso de los aneurismas, su tratamiento está, principalmente, indicado cuando se trata de aneurismas grandes o gigantes o que se presentan con manifestaciones clínicas, pudiendo realizarse un clipaje microquirúrgico que elimina el efecto compresivo inmediatamente, o un tratamiento endovascular mediante embolización que elimine la pulsatilidad y favorezca el encogimiento consecuente del aneurisma aliviando de igual manera la compresión.3
En cuanto a la recuperación visual esperada para el paciente, se ha visto que incluso pacientes que presentaban amaurosis secundaria a una neuropatía óptica compresiva lograron una recuperación total de la visión posterior a la descompresión:4 la mejoría visual postoperatoria ha sido reportada hasta en el 60% de los pacientes.2 La recuperación visual puede tomar un periodo que varía de días hasta varios meses posteriores a la intervención.4
En el metanálisis realizado por Carlson y colaboradores 2 se encontró que los factores que más predicen una recuperación visual posterior a una descompresión del nervio óptico ante una neuropatía óptica compresiva son una pérdida visual leve, un tamaño menor a 1cm de la lesión compresiva así como un disco óptico sin atrofia o palidez.
El efecto de la duración de la pérdida visual aún no es un factor claro para el pronóstico de una recuperación visual, pero parece ser que una duración de la misma menor a un año tiene mejor pronóstico que una duración más prolongada. En cuanto a los factores que implican una menor recuperación visual se encuentra un grado de pérdida visual severo y la presencia de un tumor recurrente, mientras que no se encontró que la edad o el género del paciente, así como la extensión de la lesión al canal óptico fueran factores pronósticos.2
Finalmente, es importante recordar que el reconocimiento clínico temprano, la realización de estudios de neuroimagen para evaluar el involucramiento de la vía óptica y un tratamiento intervencionista oportuno son los elementos más importantes que están en nuestras manos para evitar la pérdida visual debida a una neuropatía óptica compresiva.8
Bibliografía
- Cerovski B, Kutija MB, Vidović T, Popović-Suić S, Jandroković S, Kordić R, et al. The role of optical coherence tomography (OCT) in optic neuritis (ON). Coll Antropol [Internet]. 2013;37 Suppl 1(1):121–5. Available from: http://www.ncbi.nlm.nih.gov/pubmed/23837230
- Carlson AP, Stippler M, Myers O. Predictive factors for vision recovery after optic nerve decompression for chronic compressive neuropathy: Systematic review and meta-analysis. J Neurol Surgery, Part B Skull Base. 2013;74(1):20–38.
- Koskela E, Setälä K, Kivisaari R, Hernesniemi J, Laakso A. Neuro-ophthalmic presentation and surgical results of unruptured intracranial aneurysms-prospective helsinki experience of 142 patients. World Neurosurg. 2015;83(4):614–9.
- Fukiyama Y, Oku H, Hashimoto Y, Nishikawa Y, Tonari M, Sugasawa J, et al. Complete Recovery from Blindness in Case of Compressive Optic Neuropathy due to Unruptured Anterior Cerebral Artery Aneurysm. Case Rep Ophthalmol. 2017;8(1):157–62.
- Bhat DI, Sampath S. Anterior communicating artery aneurysm presenting as monocular blindness. Br J Neurosurg. 2011;25(5):644–6.
- Nucci C, Aiello F, Giuliano M, Colosimo C, Mancino R. Ophthalmic segment of internal carotid artery aneurysm mimicking normal tension glaucoma. Int Ophthalmol. 2016;36(6):907–14.
- Cheour M, Mazlout H, Agrebi S, Falfoul Y, Chakroun I, Lajmi H, et al. Neuropathie optique compressive secondaire à un macroadénome hypophysaire. J Fr Ophtalmol [Internet]. 2013;36(6):e101–4. Available from: http://dx.doi.org/10.1016/j.jfo.2012.08.014
- Tong J, Jefferson N, Chaganti J, Fraser CL. Compressive Optic Neuropathy from Allergic Fungal Sinusitis. Neuro-Ophthalmology. 2015;39(5):236–9.