Este artículo fue publicado y traducido bajo los términos de nuestra licencia con Jobson Healthcare Information. Queda estrictamente prohibida su reproducción total o parcial.
Por el Dr. Shan Lin
Orientación experta para determinar si realmente está presente el glaucoma.
La miopía se reconoce cada vez más como un problema importante y creciente de salud pública. Se prevé que, para 2050, casi la mitad de la población mundial será miope y aproximadamente el 10 % presentará miopía alta.¹ Aunque la prevalencia está aumentando en todo el mundo, la carga es especialmente pronunciada en Asia Oriental, con una frecuencia de entre el 80 y el 90 % entre los adultos jóvenes.²
Junto a esta tendencia, se ha documentado un aumento del riesgo de desarrollar y diagnosticar glaucoma, así como defectos estructurales y funcionales similares al glaucoma. En comparación con los ojos emétropes, a mayor grado de miopía mayor es el riesgo de glaucoma, y la miopía alta se asocia con un riesgo 7,3 veces mayor.³
Al mismo tiempo, los cambios anatómicos inherentes a la miopía alta pueden imitar muy de cerca el daño glaucomatoso, lo que complica la evaluación clínica y aumenta el riesgo de diagnósticos falsos positivos.
A continuación, analizaré los retos del diagnóstico del glaucoma en ojos con miopía alta y ofreceré consejos prácticos para distinguir la verdadera enfermedad glaucomatosa de los hallazgos relacionados con la miopía.
Mecanismos de la miopía alta
La miopía alta es un factor de riesgo independiente para el glaucoma, en gran parte debido al alargamiento axial excesivo y a la remodelación estructural resultante de la cabeza del nervio óptico y la región peripapilar. Estos cambios aumentan la susceptibilidad al estrés relacionado con la presión intraocular, y la apariencia alterada del disco óptico puede simular glaucoma, lo que complica la evaluación clínica.⁴˒⁵
Además, la miopía patológica se asocia con estiramiento y adelgazamiento de la retina, así como con atrofia coroidea que puede extenderse hacia la mácula, lo que a menudo se denomina degeneración miópica o maculopatía miópica. La fragilidad resultante del tejido retiniano puede conducir al desarrollo de complicaciones como la neovascularización coroidea y el desprendimiento de retina.
Retos diagnósticos
Determinar si realmente existe glaucoma puede resultar especialmente difícil en ojos con atrofia peripapilar y cambios en el nervio óptico asociados a la miopía. Las anomalías estructurales inducidas por la miopía pueden parecerse mucho a la neuropatía óptica glaucomatosa, y la presión intraocular suele encontrarse dentro del rango normal, lo que complica aún más el diagnóstico. Por este motivo, es importante utilizar toda la información disponible. La integración cuidadosa del aspecto de la cabeza del nervio óptico, las pruebas de campo visual, las métricas de la tomografía de coherencia óptica, los datos longitudinales y los factores de riesgo relevantes es esencial.
En los ojos con miopía alta, el disco óptico suele aparecer inclinado, agrandado y alargado, con una excavación poco profunda y una amplia zona de atrofia peripapilar circundante. Estas características pueden ocultar la verdadera pérdida del borde y dificultar la evaluación del borde neurorretiniano.
Un hallazgo que tiende a sugerir glaucoma más que cambios miópicos no glaucomatosos es la presencia de hemorragia del disco, especialmente cuando se asocia con exposición de la lámina cribosa en áreas de adelgazamiento o desplazamiento del nervio óptico.⁶ Los hallazgos del nervio óptico en ojos miopes son más indicativos de glaucoma verdadero cuando muestran progresión estructural y/o funcional consistente a lo largo del tiempo.
Pruebas de campo visual
Los defectos del campo visual son bastante comunes en la miopía alta, pero no siempre indican la presencia de glaucoma. Muchos defectos son estáticos y se deben a cambios estructurales asociados con la miopía, como el estiramiento y adelgazamiento de la retina. La afectación del campo visual central es más frecuente en estos ojos.⁷
Un estudio realizado en 1,302 ojos demostró que los defectos similares al glaucoma (es decir, defectos paracentrales, escalón nasal, defecto arcuato parcial y defecto arcuato) y los defectos relacionados con la miopía alta (es decir, punto ciego agrandado, escalón vertical, borde periférico parcial y defecto inespecífico) representaron el 10,8 % y el 15 % de todas las pruebas de campo visual únicas, respectivamente. Los defectos combinados (por ejemplo, escalón nasal con punto ciego agrandado) representaron el 0,1 % de las pruebas, mientras que los patrones de campo visual normales correspondieron al 74 %.⁸ La edad avanzada y una mayor longitud axial se asociaron tanto con defectos del campo visual similares al glaucoma como con defectos relacionados con la miopía alta; sin embargo, la mayor longitud axial tuvo un mayor efecto sobre la prevalencia de defectos similares al glaucoma que sobre los defectos relacionados con la miopía alta (p = 0,036).
Una fuente frecuente de falsos positivos es el agrandamiento del punto ciego causado por la atrofia peripapilar. La desviación del patrón asume un punto ciego normal, por lo que cualquier agrandamiento adicional puede aparecer como defectos arcuatos o pérdida paracentral. Una evaluación cuidadosa suele revelar que estos patrones son consecuencia de la atrofia retiniana y no de glaucoma.
De manera similar, la degeneración macular miópica produce defectos irregulares y parcheados que no respetan el meridiano horizontal. Los defectos que se correlacionan con áreas de atrofia retiniana en las imágenes son más probablemente consecuencia de degeneración miópica que de glaucoma. Por el contrario, los defectos glaucomatosos verdaderos suelen respetar la anatomía de la capa de fibras nerviosas de la retina (RNFL) y muestran progresión con el tiempo.
Tomografía de coherencia óptica
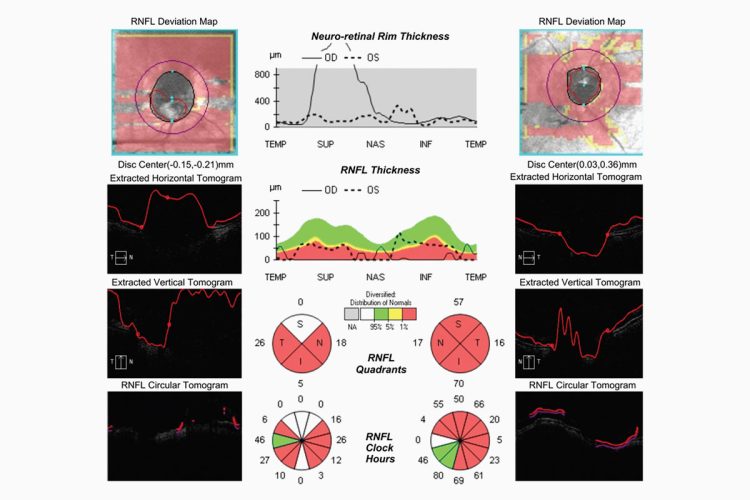
Los falsos positivos en la OCT son comunes en ojos con miopía alta. El aparente adelgazamiento de la capa plexiforme interna de las células ganglionares (GCIPL) puede reflejar una alteración de la anatomía de la RNFL secundaria a la degeneración miópica, más que una pérdida real de tejido. Un estudio que evaluó el efecto de la miopía en las mediciones del grosor de la RNFL peripapilar demostró que la longitud axial afecta el grosor promedio, mientras que la miopía influye en la distribución del grosor. Además, la miopía alta presenta patrones diferentes de distribución de la RNFL.
Con el aumento de la miopía, los picos de la RNFL en los polos superior e inferior convergen hacia el sector temporal;¹⁰ esto se ha asociado con un aumento del área de mediciones anómalas de la RNFL.¹¹
Estos cambios pueden imitar el adelgazamiento glaucomatoso y con frecuencia se encuentran dentro de los rangos típicamente asociados con glaucoma, lo que incrementa el riesgo de diagnóstico erróneo. Como siempre, es importante revisar las imágenes sin procesar y evitar basarse únicamente en los resultados codificados por colores. Repita los escaneos si es necesario.
Una característica útil de la OCT es el signo del rafe temporal en el mapa de grosor de la GCIPL. Si existe glaucoma, la pérdida de GCIPL suele respetar el meridiano horizontal, mientras que el adelgazamiento relacionado con la miopía generalmente no lo hace. Los estudios muestran que evaluar el rafe mejora la detección de glaucoma en ojos miopes.¹²
Se ha propuesto que la GCIPL inferotemporal es un parámetro macular importante para detectar glaucoma miópico preperimétrico, con un AUROC de 0,752, 0,747 y 0,737 en ojos miopes en general, no altamente miopes y altamente miopes, respectivamente.¹³ Un estudio de Yoon Jeong, MD, y colaboradores demostró resultados similares, mostrando que el grosor inferotemporal de la GCIPL tenía la mayor utilidad diagnóstica para detectar glaucoma en ojos con miopía alta.¹⁴
Los autores sugieren que las mediciones del grosor de la RNFL y de la GCIPL pueden ser más relevantes para el diagnóstico de glaucoma que los parámetros de la cabeza del nervio óptico en pacientes con miopía alta. También señalan que combinar el signo del rafe temporal con parámetros individuales de OCT puede mejorar el rendimiento diagnóstico.
Complementar las mediciones del grosor de la RNFL con mediciones tridimensionales del grosor del borde neurorretiniano (NRR) también puede mejorar la precisión diagnóstica al diferenciar entre miopía y glaucoma miópico. Un estudio en pacientes coreanos comparó estas dos métricas de OCT y reportó una tasa de falsos positivos del 26,9 % para el grosor de la RNFL y del 2,1 % para el grosor del NRR 3D (p < 0,001).¹⁵ El grosor del NRR 3D mostró la mayor precisión diagnóstica en los sectores de las 12 a las 6 y de las 9 en punto, además de mayor sensibilidad y especificidad.
Muchos dispositivos de OCT ofrecen actualmente bases de datos normativas ajustadas para miopía. Por ejemplo, Christopher K.S. Leung, MD, y colaboradores desarrollaron una base de datos específica para miopía que reduce la tasa de “enfermedad roja” en el análisis de la RNFL y mejora la especificidad diagnóstica para detectar anomalías reales de la RNFL.¹⁶ Su grupo también introdujo el Retinal Nerve Fiber Layer Optic Texture Analysis (ROTA), una herramienta que evalúa cambios sutiles de la RNFL en un campo más amplio y ayuda a diferenciar defectos glaucomatosos de los no glaucomatosos.¹⁷
Seguimiento de los pacientes
Cuando se evalúa por primera vez a un paciente con miopía alta y nervios ópticos que generan sospecha —relación copa/disco elevada, atrofia peripapilar u otras características sospechosas— a menudo es difícil determinar si realmente existe glaucoma. Los campos visuales pueden ser inconclusos, casi normales o mostrar hallazgos que imitan glaucoma. En estos casos, el seguimiento longitudinal es fundamental.
El glaucoma verdadero se define en última instancia por la progresión a lo largo del tiempo, ya sea estructural, funcional o ambas. Los pacientes sin progresión probablemente no tienen glaucoma, pero detectar cambios requiere una vigilancia cuidadosa. Esto incluye imágenes periódicas del nervio óptico y de la RNFL, así como pruebas de campo visual.
La evidencia sugiere que la progresión del glaucoma miópico puede seguir un patrón bimodal.¹⁸ Una progresión más rápida puede observarse en pacientes jóvenes, relacionada con el crecimiento continuo del ojo, y en pacientes mayores, probablemente reflejando pérdida de fibras nerviosas asociada a la edad. Reconocer estas tendencias puede ayudar a orientar la frecuencia del seguimiento y la evaluación del riesgo.
Para pacientes con glaucoma sospechoso o en etapa temprana, se recomienda un seguimiento estrecho, posiblemente cada seis meses al inicio. Las características de la OCT, como el signo del rafe temporal, pueden ser especialmente útiles para detectar cambios glaucomatosos tempranos a lo largo del tiempo. La integración de estos hallazgos estructurales con las pruebas funcionales permite una evaluación más precisa en esta población compleja.
Conclusión
La miopía es un factor de riesgo importante para el glaucoma, especialmente para el glaucoma de tensión normal, mientras que la enfermedad por cierre angular sigue siendo una consideración, particularmente en pacientes asiáticos. Con el aumento de la prevalencia mundial de la miopía, es probable que también aumente la carga de glaucoma asociado a la miopía.
Los especialistas de la salud visual deben mantener un alto nivel de vigilancia en ojos miopes. El uso de bases de datos normativas de OCT ajustadas para miopía puede mejorar la precisión diagnóstica y apoyar una mejor toma de decisiones clínicas.
El Dr. Lin es clínico-investigador y codirector de investigación en el Glaucoma Center de San Francisco. No tiene ninguna declaración financiera relevante.
Referencias:
Lin, S. C. (2024). Diagnosing glaucoma in high myopia. Review of Ophthalmology. https://www.reviewofophthalmology.com/article/diagnosing-glaucoma-in-high-myopia
- Holden BA, Fricke TR, Wilson DA, Jong M, et al. Prevalencia global de miopía y alta miopía y tendencias temporales desde 2000 hasta 2050. Oftalmología 2016;123:5:1036-1042.
2. Morgan IG, diputado francés, Ashby RS, entre otros. Las epidemias de miopía: etiología y prevención. Prog Retin and Eye Res 2018;62:134-149.
3. Wang YX, Yang H, Wei CC, Xu L, Wei WB, Jonas JB. La miopía alta como factor de riesgo para la incidencia de glaucoma de ángulo abierto a 10 años en el Estudio de la Vista de Pekín. Br J Ophthalmol 2023;107:7:935-940.
4. Chang L, Pan CW, Ohno-Matsui K, et al. Cambios en el fondo de ojo relacionados con miopía en adultos singapurenses con miopía alta. Am J Ophthalmol 2013;155:6:991-999.e1.
5. Kim TW, Kim M, Weinreb RN, et al. Cambio del disco óptico con miopía incipiente de la infancia. Oftalmología 2012;119:1:21-26.
6. Kim YK, Park KH. La lámina cribrosa se presenta defectuosos en los ojos con hemorragia discal glaucomatosa. Acta Ophthalmol 2016; 94:6:e468-473.
7. Kimura Y, Hangai M, Morooka S, etc. Defectos de la capa de fibra nerviosa retiniana en ojos muy miopes con glaucoma temprano. IOVS 2012;53:6472-6478.
8. Lin F, Chen S, Song Y, et al. Clasificación de anomalías del campo visual en ojos altamente miopes sin cambios patológicos. Ophthalmol 2022;129:7:803-812.
9. Kang SH, Hong SW, Im SK, entre otros. Efecto de la miopía sobre el grosor de la capa de fibras nerviosas retinianas medido por tomografía de coherencia óptica Cirrus HD. Invierte Ophthalmol Vis Sci 2010;51:8:4075-4083.
10. Wagner FM, Hoffmann EM, Nickels S, et al. Perfil peripapillar de la capa de fibra nerviosa retiniana en relación con el error refractivo y la longitud axial: resultados del Estudio de Salud de Gutenberg. Traducción Vis Sci Tech 2020; 9:35.
11. Leung CK, Yu M, Weinreb RN, et al. Imagen de la capa de fibras nerviosas retinianas con OCT en dominio espectral: Interpretación de los mapas RNFL en ojos miopes sanos. Invierte en Ophthalmol Vis, Sci 2012;53:9194-7200.
12. Kim YK, Yoo BW, Jeoung JW, Kim HC, Kim HJ, Park KH. Glaucoma-Capacidad diagnóstica de la diferencia de espesor entre células ganglionares y capa plexiforme interna a través del rafo temporal en ojos altamente miopes. Invierte Ophthalmol Vis Sci 2016;57:14:5856-5863.
13. Seol BR, Jeoung JW, Park KH. Capacidad de detección del glaucoma del espesor de la capa plexiforme interna de las células ganglionares maculares en glaucoma preperimétrico miope. IVOS 2015;56:13:8306-8313.
14. Jeong Y, Kim YK, Jeoung JW, entre otros. Comparación de parámetros estructurales de tomografía de coherencia óptica para el diagnóstico del glaucoma en miopía alta. JAMA Ophthalmol 2023;141:7:631-639.
15. Kim YW, Park KH. Precisión diagnóstica del grosor tridimensional del borde neurorretiniano para la diferenciación del glaucoma miope frente a la miopía. IOVS 2018;59:3655-3666.
16. Biswas S, Lin M, Leung CKS. Evaluación de una base de datos normativa miope para el análisis del grosor de la capa de fibras nerviosas retinianas. JAMA Ophthalmol 2016;134:9:1032-1039.
17. Leung CKS, Lam AKN, Weinreb RN, et al. Evaluación diagnóstica del glaucoma y neuropatía óptica no glaucomatosa mediante análisis de la textura óptica de la capa de fibras nerviosas retinianas. Ingeniería Biomédica Nacional 2022; 593-604.
18. Lee J, Shin YI, Hugh MG, et al. Tasa de progresión entre diferentes grupos de edad en glaucoma con miopía alta: un estudio de cohorte de seguimiento a 10 años. Am J Ophthalmol 2025;276:201-209.
19. Brazuna R, Amaral D, Colombini G, et al. Desafíos en el manejo del glaucoma en miopía alta tras cirugía refractiva: un informe de caso. Cureus 2026; 18:1:e100859. [Epub 5 de enero de 2026].