El tratamiento farmacológico del glaucoma continúa evolucionando con la incorporación de sistemas de liberación sostenida y nuevos agentes terapéuticos, orientados a optimizar el control de la presión intraocular y mejorar la adherencia al tratamiento.
Por Angelo P. Tanna, MD
Desde los sistemas de liberación sostenida hasta el desarrollo de fármacos dirigidos a nuevos receptores, las terapias médicas para el glaucoma continúan evolucionando. A continuación, un panorama de las novedades más recientes.
La reducción de la presión intraocular sigue siendo el único enfoque comprobado para el tratamiento del glaucoma, y hoy en día los especialistas cuentan con un mayor número de opciones farmacológicas. En los últimos años, el panorama terapéutico se ha ampliado con la incorporación de sistemas de liberación sostenida de fármacos, que ofrecen un control más constante y prolongado de la presión intraocular, reduciendo la dependencia del uso diario de gotas oftálmicas.
Paralelamente, nuevos agentes farmacológicos están surgiendo como alternativas a las terapias tradicionales. A continuación, presentamos una actualización de los avances más recientes en farmacología hipotensora ocular.
Durysta
Actualmente, el desarrollo de dispositivos de liberación sostenida está cobrando un notable impulso. Hasta la fecha, la FDA ha aprobado dos análogos de prostaglandinas para su uso en sistemas de liberación prolongada.
Aprobado en 2020 para el tratamiento del glaucoma primario de ángulo abierto y la hipertensión ocular, Durysta contiene 10 µg de bimatoprost, que se liberan de forma sostenida durante aproximadamente 90 días, logrando una reducción eficaz de la presión intraocular (PIO). Su eficacia ha demostrado ser comparable a la del timolol.
Los ensayos de Fase I/II mostraron que el efecto hipotensor ocular de Durysta se extiende más allá de los 90 días, con hasta un 28 % de los pacientes con glaucoma primario de ángulo abierto que mantuvieron la PIO controlada hasta dos años después de un único implante.¹ Resultados similares en cuanto a la reducción sostenida de la PIO al año también se observaron en los estudios ARTEMIS 1 y 2.²˒³ Estos hallazgos podrían explicarse por la alta concentración intraocular del análogo de prostaglandina y la consiguiente remodelación a largo plazo de la matriz extracelular en las vías de drenaje uveoescleral y convencional.
De acuerdo con la ficha técnica de la FDA, Durysta está aprobado para una única administración por ojo. En el estudio ARTEMIS 2, en el punto de seguimiento de seguridad extendido a los 20 meses, se reportó una pérdida de células endoteliales corneales ≥20 % en el 8,1 % de los ojos tras la implantación de tres dispositivos a intervalos de 16 semanas.³
Un análisis intermedio de Fase IIIb publicado este año mostró que el efecto reductor de la PIO se mantuvo durante más de un año en la mayoría de los pacientes, con resultados comparables tras una segunda administración.⁴ El cambio porcentual medio en la densidad de células endoteliales corneales respecto al valor basal al año fue de 4,3 ± 0,81 % en el primer ciclo y de 8,5 ± 2,22 % en el segundo ciclo.
iDose TR
Aprobado en 2023, iDose TR es un implante que contiene 75 µg de travoprost libre de conservantes, diseñado para anclarse en la malla trabecular y la esclera. En ensayos clínicos, demostró ser no inferior al timolol durante un periodo de un año.⁵
iDose TR está indicado para una única administración en pacientes con glaucoma primario de ángulo abierto (GPAA) e hipertensión ocular (HTO). El procedimiento de implantación es similar al utilizado con el dispositivo iStent Inject, requiere gonioscopía intraoperatoria y puede realizarse tanto en un quirófano convencional como en un entorno quirúrgico ambulatorio.
Los datos de seguimiento a 36 meses de los estudios de Fase III mostraron que, en comparación con el timolol, una proporción significativamente mayor de pacientes (70 % frente a 58 %) mantuvo la presión intraocular (PIO) controlada con la misma o menor cantidad de tratamiento tópico tres años después de una única administración.⁶ Entre las complicaciones observadas en los ensayos pivotales de Fase III se incluyeron uveítis y dislocación del implante, que requirió su extracción en aproximadamente el 1 % de los casos.
Este año, Glaukos anunció un programa clínico de Fase IIb/III para iDose TREX, una terapia de liberación sostenida con el doble de capacidad de fármaco en comparación con iDose TR.
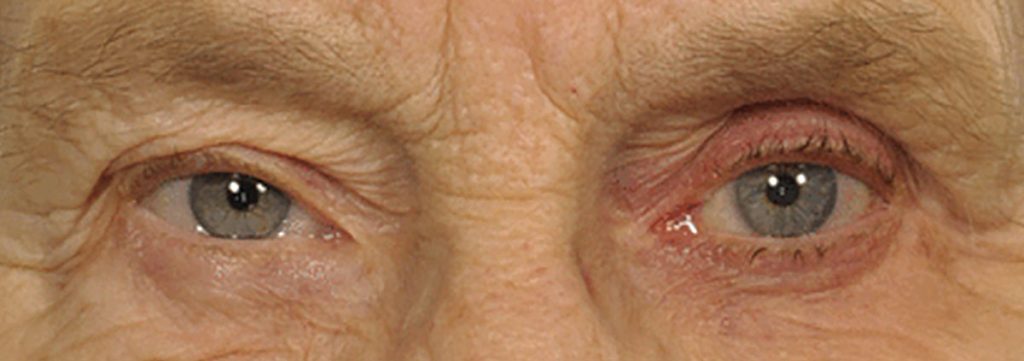
Figura 1. El tratamiento unilateral prolongado del ojo izquierdo con bimatoprost al 0,03 % dio lugar al desarrollo de periorbitopatía asociada a análogos de prostaglandinas, caracterizada por atrofia del tejido adiposo del párpado superior, profundización del surco palpebral superior, hipertricosis e hiperpigmentación periorbital.
Foto: Angelo P. Tanna, MD.
Implantes de liberación sostenida en la práctica
Dado que los fármacos no se administran en la superficie ocular, los implantes intracamerales de liberación sostenida pueden evitar algunos de los efectos adversos asociados al uso prolongado de análogos de prostaglandinas tópicos, al tiempo que ofrecen una reducción de la presión intraocular (PIO) comparable, sin las limitaciones derivadas de una baja adherencia al tratamiento. Entre las principales barreras para su adopción se encuentran el costo y su indicación de administración única.
Es importante considerar que los análogos de prostaglandinas tópicos son, en general, sencillos de utilizar con una dosificación diaria. Para la mayoría de los pacientes, el tratamiento no representa una carga significativa. Por ello, aún no está completamente claro en qué medida estas nuevas estrategias de liberación sostenida aportarán beneficios adicionales en términos de control de la enfermedad, prevención de la pérdida visual o mejora en la calidad de vida. No obstante, en pacientes con dificultades de adherencia, estos implantes representan una alternativa viable.
La falta de adherencia al tratamiento médico es difícil de detectar y cuantificar, y no siempre es posible identificar con precisión qué pacientes cumplen o no con la terapia. De hecho, estudios previos sugieren que la capacidad para evaluar la adherencia es limitada.
En este contexto, integrar estos dispositivos de liberación de fármacos en la práctica clínica plantea diversos desafíos. En opinión del autor, la mayoría de los pacientes —cuando reciben una adecuada educación y mantienen una buena relación médico-paciente— tienden a ser adherentes al tratamiento. Sin embargo, también reconoce que, en entornos académicos, es posible que se atienda a un perfil de pacientes más motivado y comprometido con el control de su enfermedad que la población general.
En cuanto a la selección de pacientes, los candidatos ideales para implantes de liberación sostenida son aquellos cuya enfermedad puede controlarse con un solo agente (como un análogo de prostaglandina), así como pacientes con baja adherencia, ya sea por edad, discapacidad, deterioro cognitivo o preferencia por evitar el uso diario de gotas. Para estos casos, los implantes de liberación sostenida pueden ser una opción adecuada. Es importante destacar que, hasta el momento, no existe evidencia de que estas estrategias sean más eficaces que la terapia tópica convencional con el mismo agente.
Existen riesgos específicos asociados al uso de implantes intraoculares de liberación sostenida. Tanto Durysta como iDose implican un riesgo de infección. En el caso de Durysta, también se ha descrito un posible impacto sobre el endotelio corneal, efecto que no se ha observado con iDose. Por ello, es fundamental que los pacientes comprendan y acepten los riesgos asociados, que van más allá del uso de gotas oftálmicas convencionales.
TABLA 1. Resumen de algunos medicamentos para glaucoma en desarrollo
| Nombre del fármaco | Fabricante | Plataforma de administración | Fase del ensayo clínico |
| LL-BMT1 | MediPrint Ophthalmics | Lente de contacto con bimatoprost | Fase III planificada |
| Glaucoma Evolute | Mati Therapeutics | Tapón lagrimal con latanoprost | Fase III planificada |
| Anillo de bimatoprost | Allergan, Dublín, Irlanda | Inserto ocular en anillo con bimatoprost | Fase II completada |
| OTX-TIC/Paxtrava | Ocular Therapeutix | Implante intracameral de travoprost (liberación sostenida) | Fase II |
| ENV515/Travoprost XR | Envisia Therapeutics | Implante intracameral de poli(esteramida) | Fase II completada |
| PA5108 | PolyActiva | Implante intracameral de latanoprost | Fase IIb |
| SpyGlass | SpyGlass Pharma | Lente intraocular con bimatoprost (liberación sostenida) | Fase I/II |
| Sepetaprost | Santen | Sepetaprost 0,002 % | Fase IIb |
En desarrollo
En los últimos años, la industria farmacéutica y la comunidad investigadora han dedicado importantes esfuerzos al desarrollo de tecnologías de liberación sostenida. Entre los dispositivos actualmente en investigación se incluyen lentes de contacto liberadoras de fármaco, tapones lagrimales, implantes de superficie ocular, implantes intracamerales y lentes intraoculares.
A continuación, se presentan algunos de los sistemas de liberación sostenida que actualmente se encuentran en desarrollo:
• LL-BMT1 (MediPrint Ophthalmics) es una lente de contacto impresa en 3D, libre de conservantes y cargada con bimatoprost. Un ensayo de Fase IIb demostró su equivalencia frente a la administración diaria de bimatoprost al 0,01 %.⁷ La compañía tiene previsto iniciar un estudio de Fase III.
• Glaucoma Evolute (Mati Therapeutics) es un tapón lagrimal liberador de latanoprost. La compañía ha completado los estudios de Fase II y, según su sitio web, planea iniciar un ensayo de Fase III en 2025.⁸
• Anillo de bimatoprost (Allergan, Dublín, Irlanda) consiste en un anillo de silicona de gran tamaño, montado sobre una estructura de soporte de polipropileno, que contiene 13 mg de bimatoprost libre de conservantes y se coloca en los fórnices conjuntivales superior e inferior. En el ensayo de Fase II a seis meses, el dispositivo fue bien tolerado y mostró una reducción clínicamente relevante de la presión intraocular (PIO); sin embargo, la magnitud de dicha reducción fue ligeramente inferior a la observada con timolol tópico administrado dos veces al día.⁹ Aunque no se evidenció en el estudio, una posible preocupación a largo plazo con este tipo de administración —basada en análogos de prostaglandina F2α— es el desarrollo de periorbitopatía asociada a prostaglandinas.
• OTX-TIC/Paxtrava (Ocular Therapeutix) es un implante intracameral de hidrogel diseñado para la liberación sostenida de travoprost. Actualmente, se encuentra en estudios clínicos de Fase II¹⁰ y ha demostrado reducciones clínicamente significativas de la PIO con un solo implante durante un periodo de hasta seis meses.¹¹
• ENV515/Travoprost XR (Envisia Therapeutics) es un implante intracameral basado en poli(esteramida). Un estudio de Fase II ya completado demostró una reducción clínicamente significativa de la PIO tras una única administración, sostenida durante un seguimiento de hasta 11 meses.¹²
• PA5108 (PolyActiva) es un implante intracameral biodegradable de latanoprost, diseñado para su inserción en la cámara anterior. El primer paciente en Estados Unidos fue reclutado en el ensayo de Fase IIb en agosto de este año. Por su parte, el estudio de Fase IIa realizado en Australia demostró una reducción sostenida de la PIO durante seis meses, con potencial para dosis repetidas.¹³
• SpyGlass (SpyGlass Pharma) es una lente intraocular (LIO) de una sola pieza con reservorios liberadores de fármaco que se deslizan sobre cada háptica para fijarse en la unión óptica-háptica de la lente. Está diseñada para su implantación en el saco capsular mediante cirugía de catarata estándar, con una duración prevista del fármaco de hasta tres años. Actualmente se encuentra en curso un estudio de Fase I/II con bimatoprost de liberación sostenida. Datos interinos positivos de seguridad y eficacia a 18 meses del primer estudio en humanos fueron presentados en ASCRS en abril de 2025. La compañía prevé avanzar hacia estudios de Fase III.¹⁴
Omidenepag isopropilo
El omidenepag isopropilo al 0,002 % (Omlonti, Ube y Santen) es un agonista selectivo del receptor prostanoide E subtipo 2 (EP2), aprobado en Estados Unidos en septiembre de 2022. Este fármaco reduce la presión intraocular (PIO) mediante la activación tanto de la vía uveoescleral como de la vía de drenaje convencional.¹⁵
La evidencia disponible respalda su uso como alternativa a los análogos de prostaglandinas tradicionales, con una menor incidencia de efectos adversos típicamente asociados a los agonistas del receptor FP, como la periorbitopatía asociada a prostaglandinas, la hipertricosis, la hiperpigmentación cutánea y los cambios en la pigmentación del iris.
Un metaanálisis reciente que incluyó 17 estudios (3.294 ojos)¹⁶ mostró que en cuatro de ellos no se observaron diferencias significativas en la reducción de la PIO entre los agonistas EP2 y los agonistas FP convencionales. Asimismo, todos los estudios reportaron reducciones significativas de la PIO respecto al valor basal con omidenepag isopropilo. Sin embargo, algunos eventos adversos oculares —como molestias, fotofobia e hiperemia— podrían presentarse con mayor frecuencia en pacientes tratados con omidenepag en comparación con aquellos tratados con análogos de prostaglandinas tradicionales.
El omidenepag puede considerarse una alternativa de primera línea en pacientes que requieren reducción de la PIO con un análogo de prostaglandina, pero que desean evitar posibles efectos adversos estéticos. No obstante, es fundamental una adecuada selección y seguimiento de los pacientes.
En uno de los dos principales ensayos clínicos realizados en Estados Unidos para su aprobación, el omidenepag mostró una eficacia ligeramente inferior a la del timolol. Además, los estudios clínicos han reportado la aparición de edema macular quístico (EMQ) en aproximadamente entre el 1 % y el 10 % de los ojos tratados.¹⁷˒¹⁸ También se han descrito casos de EMQ en ojos fáquicos con antecedentes de trabeculectomía previos al inicio del tratamiento con omidenepag.
En un estudio¹⁹ que incluyó 836 pacientes fáquicos, seis de los 86 pacientes (ocho ojos) con antecedentes de trabeculectomía e iridectomía quirúrgica desarrollaron EMQ entre seis y 11 meses después de iniciar el tratamiento con omidenepag, un hallazgo que no se observó durante la terapia previa con análogos de prostaglandina F2α.²⁰
Otras terapias en investigación
Los enfoques neuroprotectores podrían ofrecer estrategias terapéuticas independientes de la presión intraocular (PIO). Asimismo, se encuentra en investigación un nuevo análogo de prostaglandinas con actividad sobre los receptores FP y EP3. A continuación, un resumen de estas líneas de desarrollo:
• Nicotinamida. La nicotinamida, una forma de vitamina B3, es un agente en investigación particularmente prometedor en el tratamiento del glaucoma. Esta molécula desempeña un papel clave en la bioenergética mitocondrial y ha demostrado potenciales efectos neuroprotectores que podrían resultar beneficiosos en pacientes con glaucoma. No obstante, aún se requieren datos clínicos robustos que confirmen su eficacia.
La seguridad de la nicotinamida sigue siendo una preocupación relevante. En un ensayo de Fase II de pequeño tamaño, se reportó un caso de hepatotoxicidad grave que requirió ingreso en la unidad de cuidados intensivos. Aunque se trató de un evento aislado, pone de relieve la necesidad de una monitorización estricta. Otra preocupación importante es la posible autoadministración de dosis elevadas fuera del contexto de ensayos clínicos, lo que, en ausencia de controles periódicos de la función hepática, podría implicar riesgos significativos.
En este sentido, aunque el potencial terapéutico es considerable, los siguientes pasos clave incluyen demostrar su eficacia en ensayos de Fase III y establecer esquemas de dosificación seguros que puedan implementarse en la práctica clínica.
• Sepetaprost. El sepetaprost al 0,002 % es un profármaco innovador que actúa sobre los receptores de prostaglandinas FP y EP3.
En un ensayo de Fase IIb (NCT04742283), el sepetaprost demostró no inferioridad frente al maleato de timolol al 0,5 %.²¹ El estudio incluyó a 323 pacientes (68,4 % con glaucoma primario de ángulo abierto [GPAA] y 31,6 % con hipertensión ocular [HTO]), aleatorizados en una proporción 1:1 para recibir sepetaprost una vez al día (n=162) o timolol dos veces al día (n=161) en un ojo durante tres meses. La incidencia de eventos adversos fue similar entre ambos grupos (23,6 % frente a 21,3 %, respectivamente). El evento adverso más frecuente fue la hiperemia conjuntival, reportada en el 9,9 % del grupo tratado con sepetaprost y en el 2,5 % del grupo con timolol.
El sepetaprost mostró una eficacia ligeramente superior al timolol en tres de los 12 puntos de evaluación durante el periodo de estudio de tres meses.
El Dr. Angelo P. Tanna es profesor y vicepresidente del Departamento de Oftalmología, así como director del servicio de glaucoma en la Facultad de Medicina Feinberg de la Universidad Northwestern. Es consultor de Alcon y Zeiss.
Referencias:
Review of Ophthalmology. (s. f.). A medical therapy update. https://www.reviewofophthalmology.com/article/a-medical-therapy-update
1. Craven ER, Walters T, Christie WC, et al. 24-month phase I/II clinical trial of bimatoprost sustained-release implant (bimatoprost SR) in glaucoma patients. Drugs 2020;80:2:167-179.
2. Medeiros FA, Walters TR, Kolko M, et al. Phase 3, randomized, 20-month study of bimatoprost implant in open-angle glaucoma and ocular hypertension (ARTEMIS 1). Ophthalmology 2020;127:12:1627-1641.
3. Bacharach J, Tatham A, Ferguson G, et al. Phase 3, randomized, 20-month study of the efficacy and safety of bimatoprost implant in patients with open-angle glaucoma and ocular hypertension (ARTEMIS 2). Drugs 2021;81:17:2017-2033.
4. Silverstein SM, Oddone F, Kolko M, et al. Safety and longevity of intraocular pressure control after bimatoprost implant administration: Interim analysis of a phase 3b clinical trial (TRITON). Drugs 2025;85:4:557-570.
5. Sarkisian SR, Ang RE, Lee AM, et al. Travoprost intracameral implant for open-angle glaucoma or ocular hypertension: 12-month results of a randomized, double-masked trial. Ophthalmol Ther 2024;13:4:995-1014.
6. Glaukos Announces Positive Clinical Updates for its iDose® Sustained-Release Procedural Pharmaceutical Platform. Press Release. https://investors.glaukos.com/news/news-details/2025/Glaukos-Announces-Positive-Clinical-Updates-for-its-iDose-Sustained-Release-Procedural-Pharmaceutical-Platform/default.aspx. Accessed August 20, 2025.
7. MediPrint Ophthalmics Announces Promising Results from Its SIGHT-2 Phase 2b Group 1 Clinical Study. Press Release. https://mediprintlens.com/mediprint-ophthalmics-announces-promising-results-from-its-sight-2-phase-2b-group-1-clinical-study. Accessed August 20, 2025.
8. Mati Therapeutics Pipeline. https://www.matitherapeutics.com/pipeline. Accessed August 20, 2025.
9. Brandt JD, Sall K, DuBiner H, et al. Six-month intraocular pressure reduction with a topical bimatoprost ocular insert: Results of a phase II randomized controlled study. Ophthalmology 2016;123:8:1685-1694.
10. A study to evaluate the efficacy and safety of OTX-TIC (travoprost) intracameral implant for patients with open-angle glaucoma (OAG) or ocular hypertension (OHT). https://clinicaltrials.gov/study/NCT05335122. Accessed August 20, 2025.
11. Ocular Therapeutix™ Announces Positive Phase 2 PAXTRAVA™ Glaucoma Data at the American Society of Cataract and Refractive Surgery 2024 Annual Meeting. Press Release. https://www.biospace.com/ocular-therapeutix-announces-positive-phase-2-paxtrava-glaucoma-data-at-the-american-society-of-cataract-and-refractive-surgery-2024-annual-meeting. Accessed August 20, 2025.
12. Envisia Therapeutics Releases Interim ENV515 (Travoprost XR) Phase 2 Data Demonstrating 11-Month Duration-of-Action After a Single Dose in Patients With Glaucoma. Press Release. https://www.pappas-capital.com/envisia-therapeutics-releases-interim-env515-travoprost-xr-phase-2-data-demonstrating-11-month-duration-of-action-after-a-single-dose-in-patients-with-glaucoma. Accessed August 20, 2025.
13. PolyActiva Announces First Patient Enrolled in US Phase 2b Clinical Trial of its Ocular Micro Implant for Glaucoma and Ocular Hypertension. Press Release. https://firstwordpharma.com/story/5986909. Accessed August 20, 2025.
14. SpyGlass Pharma secures $75m for ophthalmic drug delivery platform. Press Release. https://www.pharmaceutical-technology.com/news/spyglass-drug-delivery-platform. Accessed August 20, 2025.
15. Sharif NA, Odani-Kawabata N, Lu F, Pinchuk L. FP and EP2 prostanoid receptor agonist drugs and aqueous humor outflow devices for treating ocular hypertension and glaucoma. Exp Eye Res 2023;229:109415.
16. Sharma S, Singh R, Balas M, Mathew DJ. Safety and efficacy of omidenepag isopropyl for elevated intraocular pressure: A systematic review and meta-analysis. Am J Ophthalmol. July 24, 2025. [Epub ahead of print].
17. Bacharach J, Brubaker JW, Evans DG, Lu F, Odani-Kawabata N, Yamabe T, Wirta DL. Omidenepag isopropyl versus timolol in patients with glaucoma or ocular hypertension: Two randomized Phase 3 trials (SPECTRUM 4 and 3). Am J Ophthalmol 2024;263:23-34.
18. Aihara M, Lu F, Kawata H, et al. Twelve-month efficacy and safety of omidenepag isopropyl, a selective EP2 agonist, in open-angle glaucoma and ocular hypertension: The RENGE study. Jpn J Ophthalmol 2021;65;810–819.
19. Cheng MH, Hwang DK, Liu CJL. Prostaglandin EP2 receptor and cystoid macular edema in phakic posttrabeculectomy eyes. JAMA Ophthalmol. August 7, 2025. [Epub ahead of print].
20. Zur D, Rachmiel R. Omidenepag isopropyl-associated cystoid macular edema after trabeculectomy. JAMA Ophthalmol. August 7, 2025. [Epub ahead of print].
21. Wirta DL, El-Harazi SM, Tepedino ME, Bacharach J. Sepetaprost 0.002% noninferiority vs. timolol 0.5% in patients with primary open-angle glaucoma or ocular hypertension: ANGEL-2. Ophthalmol Glaucoma 2025;8:4:384-392.